Jedną z metod potencjometrycznych jest miareczkowanie potencjometryczne, w którym roztwór badany (analit) jest elementem odpowiednio dobranej elektrody wskaźnikowej. Przykładem miareczkowania potencjometrycznego jest oznaczanie stężenia anionów halogenkowych za pomocą mianowanego roztworu azotanu(V) srebra. W tym celu buduje się ogniwo złożone z elektrody odniesienia i elektrody halogenosrebrowej – jako elektrody wskaźnikowej, której częścią jest analit.
Działanie elektrody halogenosrebrowej opisuje równanie (X oznacza symbol halogenu):
AgX(s) + e– ⇄ Ag(s) + X–(aq)
Potencjał tej elektrody zależy od stężenia anionów halogenkowych, które zmienia się w miarę dodawania titranta, ponieważ te jony tworzą z jonami srebra związki trudno rozpuszczalne w wodzie. Potencjał elektrody odniesienia jest niezależny od stężenia jonów w badanym roztworze, więc SEM ogniwa zależy tylko od stężenia anionów halogenkowych w analicie, co opisuje równanie:
SEM = const − 0,059logcX− (w temperaturze 298 K)
Na podstawie: W. Szczepaniak, Metody instrumentalne w analizie chemicznej, Warszawa 2008
oraz A. Skoog, D.M. West, F.J. Holler, S.R. Crouch, Podstawy chemii analitycznej, Warszawa 2007.
Jako elektroda odniesienia w opisanym miareczkowaniu potencjometrycznym może być zastosowana tzw. nasycona elektroda kalomelowa.
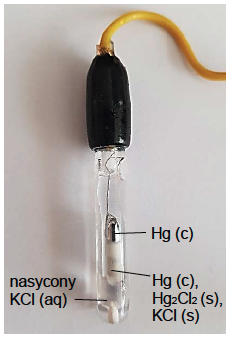
Schemat tej elektrody przedstawiono poniżej:
Hg │ Hg2Cl2 (s), KCl (roztwór nasycony)
Zasada działania tej elektrody jest taka sama jak elektrody chlorosrebrowej.
Napisz równanie reakcji elektrodowej zachodzącej w elektrodzie kalomelowej.




