Żółty roztwór chromianu(VI) potasu po zakwaszeniu zmienia barwę na pomarańczową wskutek tworzenia się jonów dichromianowych(VI) Cr2O2−7. Po wprowadzeniu jonów H3O+ powstają w pierwszej chwili jony HCrO−4, ulegające następnie kondensacji z utworzeniem jonów dichromianowych(VI).
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004, s. 893.
Przeprowadzono dwa doświadczenia.
Doświadczenie 1.
Do probówki z wodnym roztworem chromianu(VI) potasu dodawano wodny roztwór kwasu siarkowego(VI) aż do zmiany zabarwienia roztworu na pomarańczową (etap I, w wyniku którego otrzymano substancję X). Następnie do tej samej probówki dodawano wodny roztwór wodorotlenku potasu, aż do uzyskania pierwotnej barwy roztworu (etap II).
Doświadczenie 2.
Do probówki z wodnym roztworem dichromianu(VI) potasu dodawano wodny roztwór wodorotlenku potasu aż do zmiany zabarwienia roztworu na żółtą (etap I, w wyniku którego otrzymano substancję Z). Następnie do tej samej probówki dodawano wodny roztwór kwasu siarkowego(VI), aż do uzyskania pierwotnej barwy roztworu (etap II). Doświadczenia zilustrowano schematami.
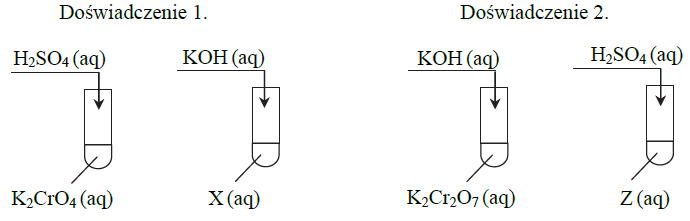
a) Napisz, w odpowiedniej kolejności, w formie jonowej skróconej równania dwóch reakcji zachodzących podczas I etapu doświadczenia 1., w których wyniku powstał roztwór substancji X
b) Napisz w formie jonowej skróconej równania reakcji zachodzących podczas I i II etapu doświadczenia 2.
c) Sformułuj wniosek dotyczący trwałości chromianów(VI) i dichromianów(VI) w zależności od środowiska reakcji.




