Jedną z metod potencjometrycznych jest miareczkowanie potencjometryczne, w którym roztwór badany (analit) jest elementem odpowiednio dobranej elektrody wskaźnikowej. Przykładem miareczkowania potencjometrycznego jest oznaczanie stężenia anionów halogenkowych za pomocą mianowanego roztworu azotanu(V) srebra. W tym celu buduje się ogniwo złożone z elektrody odniesienia i elektrody halogenosrebrowej – jako elektrody wskaźnikowej, której częścią jest analit.
Działanie elektrody halogenosrebrowej opisuje równanie (X oznacza symbol halogenu):
AgX(s) + e– ⇄ Ag(s) + X–(aq)
Potencjał tej elektrody zależy od stężenia anionów halogenkowych, które zmienia się w miarę dodawania titranta, ponieważ te jony tworzą z jonami srebra związki trudno rozpuszczalne w wodzie. Potencjał elektrody odniesienia jest niezależny od stężenia jonów w badanym roztworze, więc SEM ogniwa zależy tylko od stężenia anionów halogenkowych w analicie, co opisuje równanie:
SEM = const − 0,059logcX− (w temperaturze 298 K)
Na podstawie: W. Szczepaniak, Metody instrumentalne w analizie chemicznej, Warszawa 2008
oraz A. Skoog, D.M. West, F.J. Holler, S.R. Crouch, Podstawy chemii analitycznej, Warszawa 2007.
Przykładem elektrody halogenosrebrowej jest elektroda chlorosrebrowa:
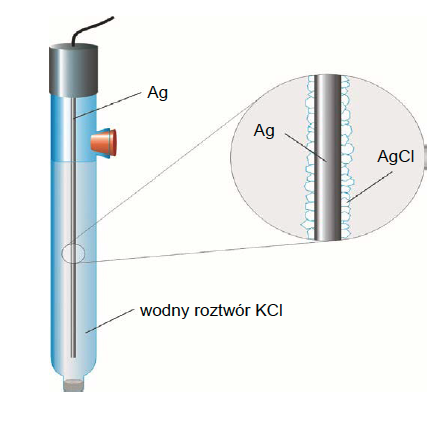
Na podstawie: E. Generalic, https://glossary.periodni.com/glossary.php?en=silver%2Fsilver-chloride+electrode [dostęp: 15.07.2020]
Działanie elektrody chlorosrebrowej opisuje równanie:
AgCl(s) + e− ↔ Ag(s) + Cl− (aq)
Potencjał tej elektrody zależy od stężenia jonów chlorkowych w roztworze, który stanowi jej element, i wyraża się równaniem: EAg/AgCl = EoAg/AgCl −0,059logcCl− (w temperaturze 298 K). Przygotowano dwie elektrody chlorosrebrowe: elektroda I zawierała wodny roztwór chlorku potasu o stężeniu równym 0,10 mol ∙dm–3, a elektroda II – wodny roztwór tej samej soli o stężeniu równym 0,01 mol ∙dm–3
Rozstrzygnij, która elektroda chlorosrebrowa (I czy II) ma – w tej samej temperaturze – wyższy potencjał. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie:




