| II. Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania problemów. Zdający: 5) wykorzystuje wiedzę i dostępne informacje do rozwiązywania problemów chemicznych […]; 7) wykonuje obliczenia dotyczące praw chemicznych. |
I. Atomy, cząsteczki i stechiometria chemiczna. Zdający: 5) dokonuje interpretacji jakościowej i ilościowej równania reakcji w ujęciu molowym, masowym i objętościowym (dla gazów); 6) wykonuje obliczenia […] dotyczące: liczby moli oraz mas substratów i produktów (stechiometria wzorów i równań chemicznych), objętości gazów […]. |
Zasady oceniania
2 pkt – zastosowanie poprawnej metody, poprawne wykonanie obliczeń i podanie wyniku w procentach.
1 pkt – zastosowanie poprawnej metody, ale:
- popełnienie błędów rachunkowych.
LUB
- niepodanie wyniku w procentach (z błędną jednostką).
0 pkt – zastosowanie błędnej metody obliczenia albo brak rozwiązania.
Przykładowe rozwiązanie
Przyjmujemy, że mieszanina wiórków magnezu i miedzi składa się z 8 moli Mg i 3 moli Cu, więc jej masa wynosi: m = 8 mol · 24 g·mol–1 + 3 mol · 64 g·mol–1 = 384 g
W reakcji tej mieszaniny wiórków metali wydzieliło się 8 moli wodoru.
Druga mieszanina wiórków metali (Al i Ag) ma również masę 384 g i pod działaniem HCl przebiega w niej reakcja opisana równaniem: 2Al + 6HCl → 2AlCl3 + 3H2
W reakcji tej też wydziela się 8 moli wodoru, więc masę glinu w mieszaninie wiórków można obliczyć z proporcji:
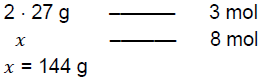
Zawartość glinu w mieszaninie wiórków: (144 g/384 g) · 100 % = 37,5 % ≅ 38 %


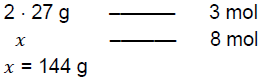



Dlaczego 8 moli wodoru