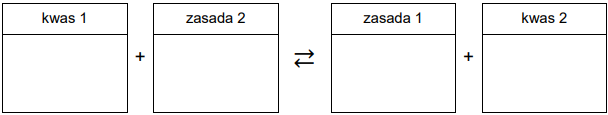
Lecytyny są naturalnymi związkami o dużym znaczeniu biologicznym. Znalazły one zastosowanie m.in. w przemyśle spożywczym jako emulgatory, czyli substancje stabilizujące emulsję. Ogólną strukturę lecytyny przedstawia wzór:

Symbolami –R1 i –R2 oznaczono grupy węglowodorowe. Najczęściej występujące łańcuchy węglowodorowe w cząsteczkach lecytyny wymieniono w poniższej tabeli.
| –R1 |
–R2 |
–C15H31
–C17H35
–C17H33 |
–C17H33
–C17H31
–C17H29 |
Cząsteczka lecytyny zawsze zawiera co najmniej jeden nienasycony łańcuch węglowodorowy.
Na podstawie: E. Siepka, Ł. Bobak, W. Gładkowski, Charakterystyka aktywności biologicznej fosfolipidów żółtka, „Żywność. Nauka. Technologia. Jakość”, 2015, nr 2(99).
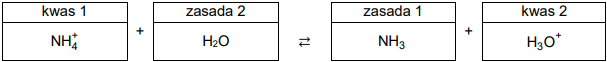
Próbkę lecytyny ogrzewano z wodnym roztworem wodorotlenku sodu. Zaszła reakcja chemiczna, zgodnie ze schematem:

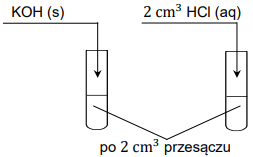
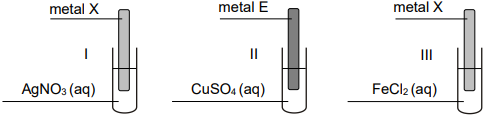
W celu potwierdzenia obecności wybranych produktów reakcji mieszaninę poreakcyjną podzielono na trzy części i umieszczono w ponumerowanych probówkach. Do probówki 1. dodano wodę bromową, do 2. – zalkalizowaną świeżo strąconą zawiesinę wodorotlenku miedzi(II), natomiast do probówki 3. dodano kilka kropel wodnego roztworu chlorku wapnia.
Uzupełnij zdanie. Określ stosunek liczby moli wodorotlenku sodu do liczby moli lecytyny w opisanej reakcji.
Stosunek liczby moli wodorotlenku sodu do liczby moli lecytyny jest równy ……..… : …………
Uzupełnij tabelę. Wpisz w odpowiednie miejsca:
- obserwowane efekty reakcji
- wzory produktów (cząsteczki lub jednego wybranego jonu), których obecność była przyczyną obserwowanych efektów (w miejsce grup –R1 albo –R2 wpisz wzór odpowiedniej grupy węglowodorowej).
| Numer probówki |
Obserwowany efekt reakcji |
Wzór wykrytej cząsteczki lub jonu |
| 1 |
odbarwienie roztworu |
|
| 2 |
|
|
| 3 |
|
PO43- LUB C17H35COO– |