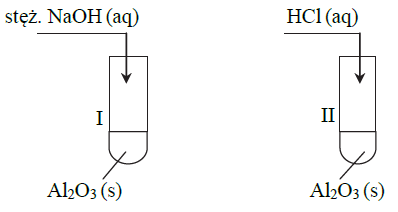
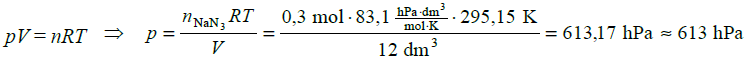Poprawne odpowiedzi
a) 1. I, III
2. I, III
3. III, IV
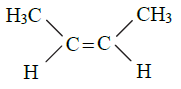
b) CH3COCH3 lub 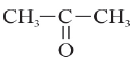
c) 1. F
2. P
3. F
Wskazówki do rozwiązania zadania
a)
W informacji podano wzory półstrukturalne związków organicznych zaliczanych do alkanów, cykloalkanów, alkenów i alkinów. Na tej podstawie można wyprowadzić wzór sumaryczny każdego węglowodoru, a potem wzór ogólny grupy związków.
| alkan |
cykloalkan |
alken |
alkin |
| C3H8 |
C3H6 |
C3H6 |
C3H4 |
| CnH2n+2 |
CnH2n |
CnH2n |
CnH2n-2 |
Z podanego zestawienia wynika, że wzór CnH2n mają cykloalkany i alkeny, do których należą związki oznaczone numerami I i III, są to propen i cyklopropan. Związki te są izomerami konstytucyjnymi, bo mając ten sam wzór sumaryczny, różnią się budową. Reakcjami charakterystycznymi dla związków organicznych nasyconych są reakcje substytucji, dla związków nienasyconych charakterystyczne są reakcje addycji.
b)
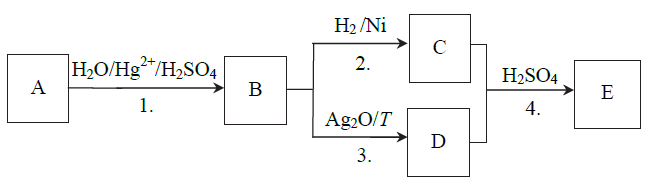
Związek II czyli propyn ulega reakcjom addycji (przyłączania). Reakcja addycji zachodzi kosztem wiązania potrójnego, końcowy produkt jest związkiem nasyconym. Przyłączenie cząsteczek wody do cząsteczek propynu w obecności soli rtęci i kwasu siarkowego(VI) prowadzi do otrzymania ketonu, w tym wypadku do propanonu o wzorze CH3COCH3.
c)
Wiedząc, do jakiej grupy węglowodorów należą poszczególne związki i jakie reakcje są dla nich charakterystyczne, można stwierdzić, czy podane zdania są prawdą, czy fałszem. Addycja wodoru do węglowodorów nienasyconych prowadzi do powstania alkanu. Cząsteczka propenu ma 1 wiązanie podwójne i może przyłączyć tylko 1 cząsteczkę wodoru. Cząsteczka propynu ma wiązanie potrójne, może więc przyłączyć 2 cząsteczki wodoru, a przyłączając tylko 1, przekształci się w propen, a nie propan. Propen ulega utlenieniu, dając alkohol dihydroksylowy. Całkowite spalanie węglowodorów prowadzi do otrzymania tlenku węgla(IV) i wody. Najwięcej cząsteczek wody powstanie ze spalenia węglowodoru, którego cząsteczka zawiera największą liczbę atomów wodoru, a więc propanu, a nie cyklopropanu. Przebieg reakcji spalania ilustrują poniższe równania:
C3H8 + 5O2 → 3CO2 + 4H2O
C3H6 + 4,5O2 → 3CO2 + 3H2O
C3H4 + 4O2 → 3CO2 + 2H2O
| Wymagania ogólne |
II. Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania problemów. Uczeń rozumie podstawowe pojęcia […]; |
| Wymagania szczegółowe |
9. Węglowodory. Uczeń: 7) opisuje właściwości alkanów, na przykładzie następujących reakcji: spalanie, podstawianie (substytucja) […]; 8) opisuje właściwości alkenów, na przykładzie następujących reakcji: przyłączanie (addycja): H2, […], przewiduje produkty reakcji przyłączenia cząsteczek niesymetrycznych do niesymetrycznych alkenów na podstawie reguły Markownikowa […]; |
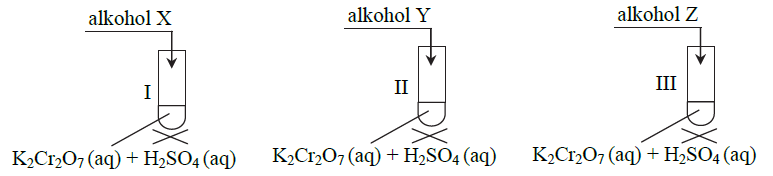


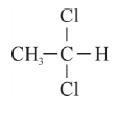
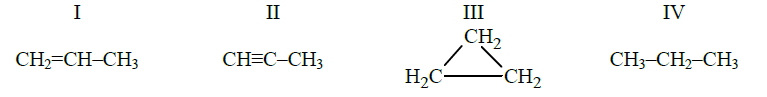
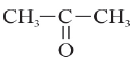
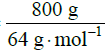 = 12,5 mola
= 12,5 mola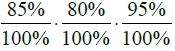 ⋅ 100% 64,6%
⋅ 100% 64,6%
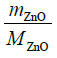
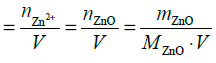
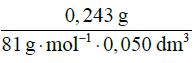 = 0,06 mol ⋅ dm–3
= 0,06 mol ⋅ dm–3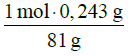 = 0,003 mola Zn2+
= 0,003 mola Zn2+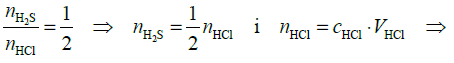
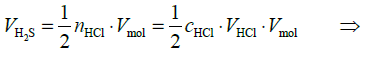
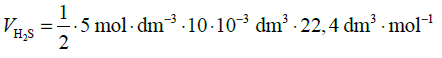
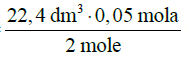 = 0,56 dm3 560 cm3
= 0,56 dm3 560 cm3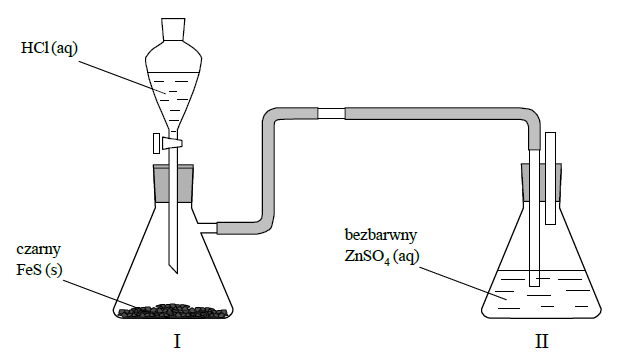
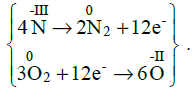 Po przekształceniu tego formalnego zapisu do postaci cząsteczkowej, otrzymujemy ostateczną formę cząsteczkową równania:
Po przekształceniu tego formalnego zapisu do postaci cząsteczkowej, otrzymujemy ostateczną formę cząsteczkową równania: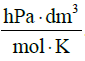
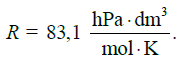
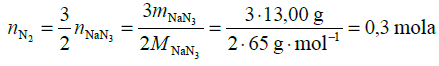
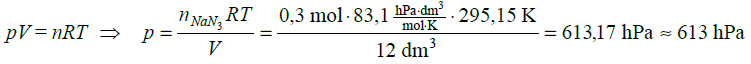
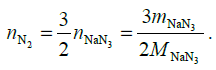 Obliczamy masę molową azydku sodu, podstawiamy do wyrażenia na liczbę moli azotu i obliczamy liczbę moli azotu (równą 0,3 mola). Mamy w ten sposób wszystkie wielkości potrzebne do obliczenia ciśnienia: liczbę moli i objętość gazu oraz temperaturę (tę wielkość trzeba wyrazić w kelwinach: T = (273,15 + 22,00) K = 295,15 K). Przekształcamy równanie Clapeyrona tak, aby otrzymać wyrażenie na ciśnienie i podstawiamy do niego dane, zaokrąglając wynik wyrażony w hPa do jedności:
Obliczamy masę molową azydku sodu, podstawiamy do wyrażenia na liczbę moli azotu i obliczamy liczbę moli azotu (równą 0,3 mola). Mamy w ten sposób wszystkie wielkości potrzebne do obliczenia ciśnienia: liczbę moli i objętość gazu oraz temperaturę (tę wielkość trzeba wyrazić w kelwinach: T = (273,15 + 22,00) K = 295,15 K). Przekształcamy równanie Clapeyrona tak, aby otrzymać wyrażenie na ciśnienie i podstawiamy do niego dane, zaokrąglając wynik wyrażony w hPa do jedności: