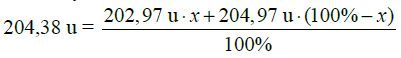W tabeli zestawiono właściwości fizyczne borowców.
| Nazwa pierwiastka | Ogólna konfiguracja elektronów walencyjnych w stanie podstawowym | Rozpowszechnienie w skorupie ziemskiej, % | Gęstość, g · cm–3 |
Temperatura topnienia, K |
| bor | ns2np1 | 1,0 ⋅ 10−4 | 2,34 | 2570,00 |
| glin | 8,23 | 2,70 | 933,47 | |
| gal | 1,9 ⋅ 10−4 | 5,91 | 302,91 | |
| ind | 4,5 ⋅ 10−5 | 7,31 | 429,75 | |
| tal | 8,5 ⋅ 10−5 | 11,85 | 577,00 |
Większość pierwiastków 13. grupy układu okresowego stanowi mieszaninę 2 trwałych izotopów, np. tal występuje w przyrodzie w postaci 2 izotopów o masach równych 202,97 u i 204,97 u. Bor jest pierwiastkiem niemetalicznym, podczas gdy pozostałe pierwiastki tej grupy są metalami. Glin i tal mają typowe sieci metaliczne o najgęstszym ułożeniu atomów, gal i ind tworzą sieci rzadko spotykane u metali. Te różnice w strukturze powodują różnice w twardości i temperaturach topnienia. Glin jest kowalny i ciągliwy; gal jest twardy i kruchy, natomiast ind należy do najbardziej miękkich pierwiastków – daje się kroić nożem, podobnie jak tal. Elementarny bor wykazuje bardzo wysoką temperaturę topnienia, co jest spowodowane występowaniem w jego sieci przestrzennej silnych wiązań kowalencyjnych. Bor można otrzymać w reakcji redukcji tlenku boru metalicznym magnezem użytym w nadmiarze. Otrzymany tą metodą preparat zawiera 98% boru, natomiast 2% stanowią zanieczyszczenia takie, jak tlenek magnezu i nadmiar użytego do reakcji magnezu. Czysty krystaliczny bor można otrzymać między innymi przez rozkład termiczny jodku boru. Krystaliczny bor ma barwę czarnoszarą, wykazuje dużą twardość i jest złym przewodnikiem elektryczności; charakteryzuje się małą aktywnością chemiczną – nie działa na niego wrzący kwas solny ani kwas fluorowodorowy.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004, s. 760–793; J. Sawicka i inni, Tablice chemiczne, Gdańsk 2002, s. 202.
Z układu okresowego pierwiastków odczytaj z dokładnością do drugiego miejsca po przecinku średnią masę atomową talu i oblicz, jaki procent atomów talu występujących w przyrodzie stanowią atomy o masach atomowych podanych w informacji.