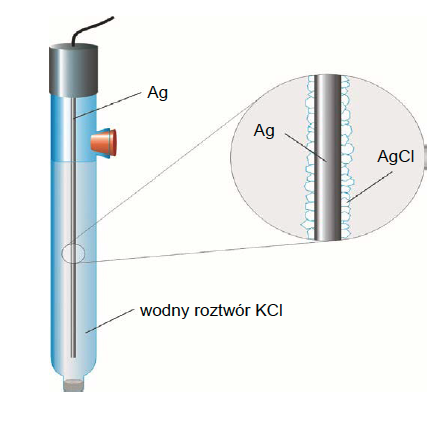
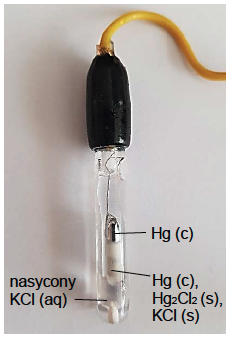
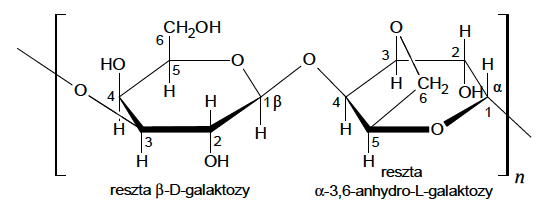
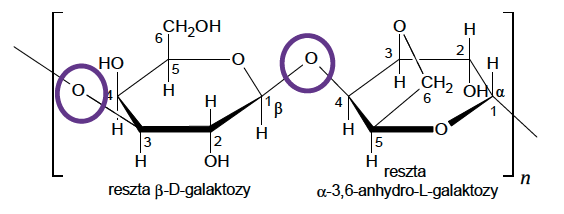
Jedną z metod potencjometrycznych jest miareczkowanie potencjometryczne, w którym roztwór badany (analit) jest elementem odpowiednio dobranej elektrody wskaźnikowej. Przykładem miareczkowania potencjometrycznego jest oznaczanie stężenia anionów halogenkowych za pomocą mianowanego roztworu azotanu(V) srebra. W tym celu buduje się ogniwo złożone z elektrody odniesienia i elektrody halogenosrebrowej – jako elektrody wskaźnikowej, której częścią jest analit.
Działanie elektrody halogenosrebrowej opisuje równanie (X oznacza symbol halogenu):
AgX(s) + e– ⇄ Ag(s) + X–(aq)
Potencjał tej elektrody zależy od stężenia anionów halogenkowych, które zmienia się w miarę dodawania titranta, ponieważ te jony tworzą z jonami srebra związki trudno rozpuszczalne w wodzie. Potencjał elektrody odniesienia jest niezależny od stężenia jonów w badanym roztworze, więc SEM ogniwa zależy tylko od stężenia anionów halogenkowych w analicie, co opisuje równanie:
SEM = const − 0,059logcX− (w temperaturze 298 K)
Na podstawie: W. Szczepaniak, Metody instrumentalne w analizie chemicznej, Warszawa 2008
oraz A. Skoog, D.M. West, F.J. Holler, S.R. Crouch, Podstawy chemii analitycznej, Warszawa 2007.
Przeprowadzono miareczkowanie potencjometryczne w celu oznaczenia stężenia anionów chlorkowych i jodkowych w badanym roztworze. Próbkę roztworu o objętości V0 = 10,00 cm3 rozcieńczono wodą do objętości 50,00 cm3. Ten rozcieńczony roztwór stanowił analit i został użyty jako część halogenosrebrowej elektrody wskaźnikowej. Z tej elektrody oraz elektrody odniesienia zbudowano ogniwo, po czym zmierzono jego SEM. Następnie do analitu stopniowo wkraplano roztwór azotanu(V) srebra o stężeniu cAgNO3 = 0,05mol * dm-3 . Po dodaniu każdej porcji titranta mierzono SEM ogniwa. W czasie miareczkowania wytrącały się kolejno osady halogenków srebra, czemu towarzyszyły dwie duże zmiany mierzonej siły elektromotorycznej odpowiadające dwóm punktom równoważnikowym miareczkowania.
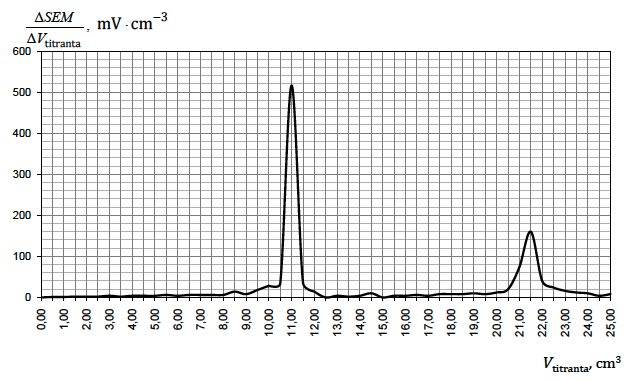
Punkt równoważnikowy I odpowiadał momentowi, w którym liczba dodanych moli jonów Ag+ była równa liczbie moli jonów halogenkowych wytrącających się jako pierwsze. Analogicznie przebiegało oznaczenie drugiego rodzaju jonów halogenkowych i momentowi, w którym zaszła równość liczb moli, odpowiadał punkt równoważnikowy II.
Aby wyznaczyć objętość titranta w I i II punkcie równoważnikowym miareczkowania, dla każdej dodanej porcji titranta Δ Vtitranta obliczono zmianę siły elektromotorycznej ogniwa ΔSEM, a następnie sporządzono wykres ΔSEM/Δ Vtitranta jako funkcji Vtitranta.
W temperaturze 298 K iloczyn rozpuszczalności chlorku srebra Kso[AgCl]= 1,6⋅10−10 , a jodku srebra – Kso[AgI]=1,5⋅10−16 .
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2007.
Oblicz stężenie molowe jonów chlorkowych w roztworze, którego próbkę o objętości V0 = 10,00 cm3 pobrano do miareczkowania.
Obliczenia: