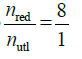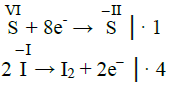Żelazo jest pierwiastkiem chemicznym, którego atomy występują w przyrodzie w postaci 4 trwałych odmian izotopowych. Najbardziej rozpowszechnioną odmianę stanowią nuklidy o liczbie masowej 56.
Silnie rozdrobnione żelazo zapala się samorzutnie w powietrzu. Produktem utleniania żelaza w wysokich temperaturach jest magnetyt, Fe3O4. Powstaje on także w czasie spalania żelaza w czystym tlenie (reakcja 1.). Oprócz tlenku Fe3O4 żelazo tworzy jeszcze 2 inne tlenki: FeO i Fe2O3. W podwyższonych temperaturach żelazo reaguje również z parą wodną według równania:
3Fe + 4H2O → Fe3O4 + 4H2
Roztwarzając czyste żelazo w kwasie solnym, uzyskuje się wodny roztwór chlorku żelaza(II) (reakcja 2.), natomiast działając gazowym chlorem na żelazo w podwyższonej temperaturze, uzyskuje się chlorek żelaza(III) (reakcja 3.). Pary chlorku żelaza(III) kondensują, tworząc ciemnobrunatne kryształy dobrze rozpuszczalne w wodzie.
Żelazo ma zdolność zastępowania mniej aktywnych metali w ich roztworach. Przebiega wtedy reakcja opisana schematem:
MeI + Me2+II → Me2+I + MeII
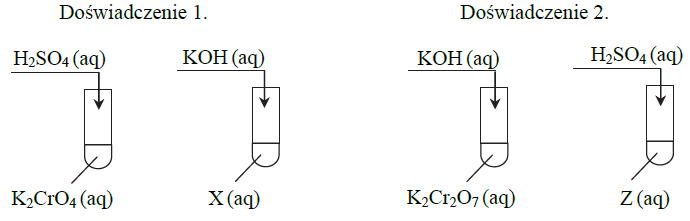
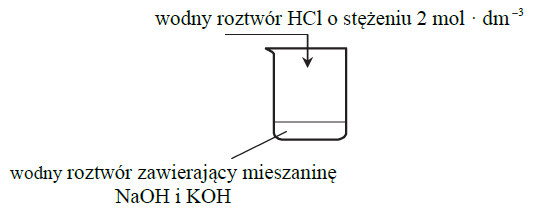
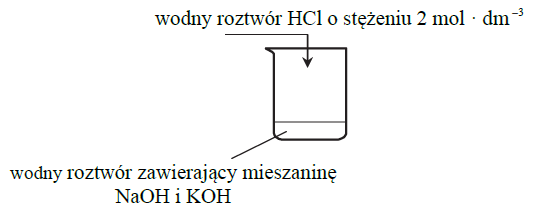
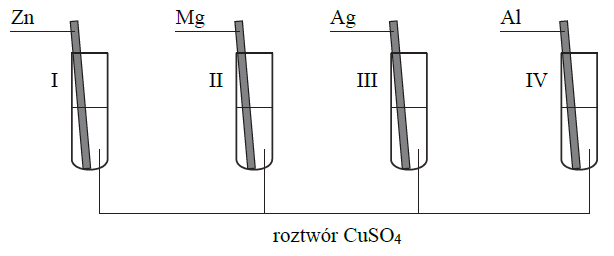
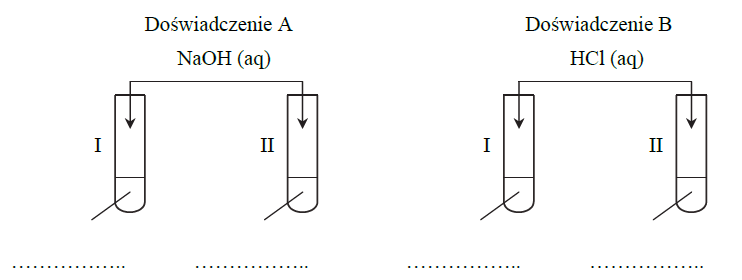
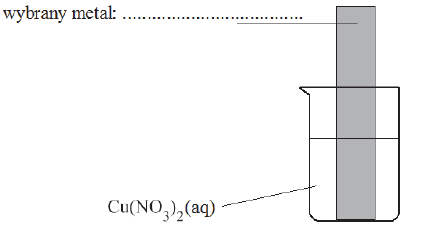
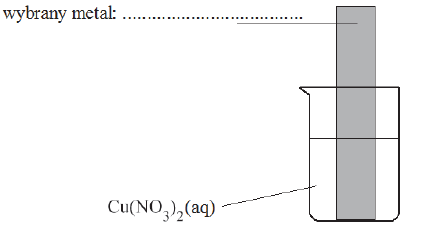
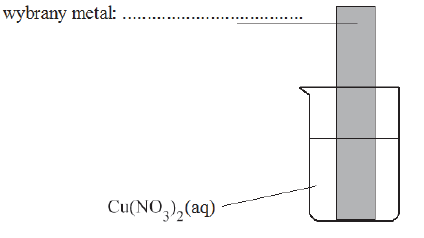
Powyższa przemiana zachodzi także podczas doświadczenia zilustrowanego rysunkiem:

Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004, s. 917–934; M. Sienko, R. Plane, Chemia, podstawy i zastosowania, Warszawa 1996, s. 542–550; J. Sawicka i inni, Tablice chemiczne, Gdańsk 2002, s. 202.
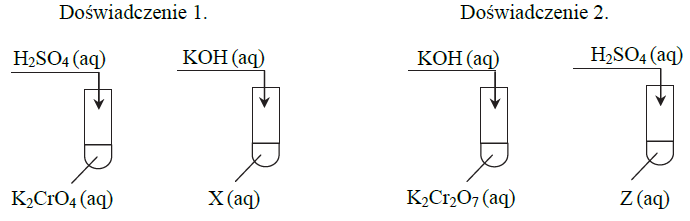
Skorzystaj z opisu doświadczenia, a następnie wpisz do tabeli literę P, jeżeli zdanie jest prawdziwe, lub literę F – jeśli jest fałszywe.
| Zdanie | P/F |
| 1. Podczas doświadczenia przebiegła reakcja chemiczna opisana równaniem: Fe + Cu2+ → Fe2+ + Cu | |
| 2. Podczas przebiegu doświadczenia płytka pokryła się czerwonobrunatnym nalotem, a roztwór zmienił barwę z niebieskiej na zielonkawą. | |
| 3. Gdyby po zakończeniu doświadczenia płytkę wyjęto z roztworu, a następnie wysuszono i zważono, to okazałoby się, że jej masa zmniejszyła się. |


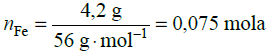
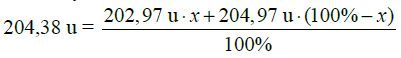
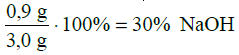
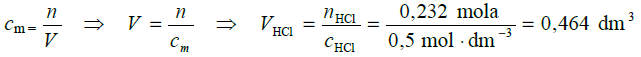
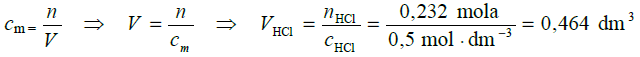
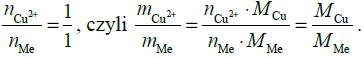
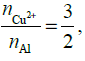 , a więc nCu2+ =
, a więc nCu2+ = 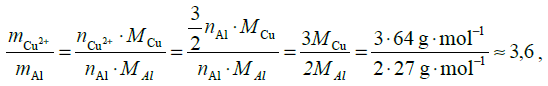
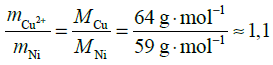 , czyli masa roztworzonego niklu jest nieznacznie mniejsza od masy wydzielonej miedzi;
, czyli masa roztworzonego niklu jest nieznacznie mniejsza od masy wydzielonej miedzi;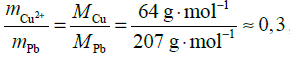 , czyli masa roztworzonego ołowiu jest znacznie większa od masy wydzielonej miedzi. Metalem tym był więc ołów.
, czyli masa roztworzonego ołowiu jest znacznie większa od masy wydzielonej miedzi. Metalem tym był więc ołów.